کلیات
در تمام روش های کروماتوگرافی جریانی از یک فاز متحرک از کنار یا درون فاز ساکنی عبور کرده ترکیبات مختلف موجود در فاز متحرک بر حسب شدت تمایل خود به فاز ساکن از هم جدا می شوند . به عبارت دیگر فاز ساکن بعضی از اجسام را محکم تر نگه می دارد و بعضی را با شدت کمتر بنابر این سرعت حرکت اجزا مختلف موجود در فاز متحرک روی فاز ساکن با یکدیگر متفاوت است . بعضی سریع تر عبور می کنند و بعضی کندتر و به این ترتیب اجزا از هم جدا می شوند. در واقع جدا شدن ترکیبات مختلف بر اساس جذب سطحی آنها توسط فاز ساکن است. فاز ساکن ممکن است جامد یا مایع و فاز متحرک مایع یا گاز باشد. روش های کروماتوگرافی را میتوان به طرق مختلف تقسیم بندی نمود.
روش های تقسیم بندی متداول به ترتیب زیر است:
- بر اساس ماهیت فاز متحرک:
- بر اساس ماهیت فاز ساکن :
- مایع: گروماتوگرافی گاز مایع GLC
- جامد: کروماتوگرافی گاز جامد GSC
- بر حسب تکنیک به کار رفته
- کروماتوگرافی ستونی
- TLC
- کروماتوگرافی کاغذی
الف – کروماتوگرافی بر روی غشا نازک (TLC) (TLC) عبارت است از جدا کردن و مشخص نمودن اجسام شیمیایی به کمک حرکت حلال از روی یک طبقه نازک جاذب این لایه نازک بر روی شیشه یا جسم دیگری که خود اثری بر جدا سازی ندارد، کشیده می شود.
بدین منظور جاذب را با حلال مناسبی که غالبا آب است ، به صورت دوغابه در می آورند و آن را بر روی صفحات شیشه می مالند. سپس صفحات را در هوای آزاد خشک کرده و به منظور فعال کردن آنها را در آون قرار میدهند. نمونه را نیز که در حلال مناسبی نظیر کلروفرم یا متانول حل و به صورت لکه بر روی ابتدای صفحه (TLC) قرار می دهند. آنگاه صفحه محتوای نمونه را در تانک حاوی حلال فاز متحرک) قرار میدهند حلال تدریجا بالا رفته، اجزای موجود را متناسب با وزن مولکولی و ساختمان شیمیایی و رابطه آنها با حلال و جاذب در فواصل معین نسبت به محل لکه اصلی جدا می کند که از روی میزان حرکت جسم از نقطه حرکت (RI) و مقایسه با لکه شاهد استاندارد میتوان برای تشخیص لکه ها استفاده نمود. TLC در مقایسه با سایر روشهای کروماتوگرافی روشی ساده و ارزان بوده و از حساسیت خوبی برخوردار می باشد.
ب – کروماتوگرافی بر روی غشا نازک با کارایی بالا (HPTLC) وجود مواد ، دستگاه و روشهای جدید موجب ایجاد HPTLC شده است. قدرت تفکیک صفحات HPTLC خیلی زیاد تر از صفحات معمولی میباشد زیرا ذرات آن خیلی ریزتر ( ۲ تا ۷ میکرومتر ) و محدوده توزیع ذرات کم است. این نکته باعث قابلیت انجام مجدد آزمون ، حساسیت بیشتر و تعیین مقدار دقیق تر شده است. ایجاد دستگاه های خودکار جهت قرار دادن محلولها بر روی صفحات و دانسیته سنج موجب کاربرد وسیع آن در تجزیه داروها شده است. در جدول ذیل HPTLC و TLC مقایسه شده است:
|
شرایط
|
TLC
|
HPTLC
|
|
ابعاد صفحه ( سانتی متر)
|
20×20 |
10×10 |
| اندازه ذرات )میکرومتر) |
20
|
5
|
| حجم نمونه (میکرولیتر) |
1-10
|
<1/0
|
| تعداد نمونه ها برای هر صفحه |
10-15
|
30-40
|
| حد آشکار سازی جذبی ( نانوگرم) |
10-100
|
5- 5/0
|
|
تکرار پذیری تعیین مقدار( ضریب تغییرات)
|
5% |
2% – 3%
|
ج – کروماتوگرافی با کارایی بالا (HPLC)
HPLC یک روش کروماتوگرافی ستونی میباشد که در آن جریانی از فاز متحرک از یک ستون محتوی ذرات فاز ساکن فشرده عبور می نماید. در حین عبور فاز متحرک اجزا مخلوطی که باید از هم جدا گردند. بر اساس تمایل به فاز ساکن و متحرک جدا می شوند. پرواضح است. اجسامی که به فاز ساکن تمایل بیشتر نشان دهند، مدت بیشتری در ستون میمانند و در واقع زمان باز داری بالایی از خود نشان میدهند و برعکس اجسامی که به فاز متحرک تمایل بیشتری دارند، سریع تر از ستون شسته میشوند و زمان بازداری کمتری از خود نشان می دهند.
در این تکنیک بر حسب این که ماهیت فاز ساکن چه باشد، مکانیزم جداسازی و نوع تکنیک HPLC متفاوت خواهد بود. به عنوان مثال چنانچه فاز ساکن از ذرات قطبی ( سیلیکاژل ) تشکیل شده باشد، تکنیک مزبور فاز نرمال (Normal Phase) و چنانچه این فاز غیر قطبی باشد (C18) تکنیک فاز معکوس (Reversed Phase) خواهد بود. در تکنیکهای فوق جدا سازی بر پایه جذب سطحی نمونه با فاز ساکن میباشد.
د- در کروماتوگرافی تبادل یونی فاز ساکن یک ماده تبادل کننده یونی است ( معمولا رزین) و بر مبنای برهم کنش یون جز نمونه و یونهای تعویض شونده رزین ، جداسازی امکان پذیر است.
ه- در کروماتوگرافی طردی ( Exclusion Chromatography) از فاز ساکن ژله ای که منافذ متعددی دارند استفاده میشود و مولکول ها بر مبنای اندازه و شکل جدا میگردند. مولکولهای بزرگ تر که توان ورود به منافذ را ندارند، سریع تر از ستون خارج و مولکولهای کوچک تر که در داخل منافذ نفوذ میکنند دیرتر از ستون خارج میشوند.
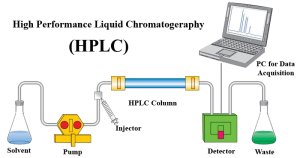
اجزا اصلی یک دستگاه HPLC متشکل از یک پمپ فشار قوی ، یک مخزن حلال ( مخزن فاز متحرک) ، یک ستون محتوی فاز ساکن فشرده، یک واحد تزریق نمونه یک آشکار ساز و نیز یک دستگاه ثبات است. در شکل ذیل نحوه ارتباط اجزا نسبت به هم نمایش داده شده است.
چگونه میتوان کارایی یک ستون HPLC را افزایش داد؟
اگر میخواهید مدت زمان کارکرد مفید و کارآیی یک ستون را افزایش دهید و مشکلات آنالیتیکال ناشی از ستون را به حداقل برسانید.
به توصیه های زیر توجه کنید.
۱ – هرستون را برای یک آنالیز خاص اختصاص دهید .
۲ – حتی الامکان از صافی سر راهی در مسیر فاز متحرک قبل از ستون اصلی و حتی پیش از ستون محافظ ( guard column ) استفاده کنید .
۳- از ستون محافظ استفاده کنید و گهگاه آن را خارج از مسیر ستون اصلی شستشو دهید.
4- توصیه میشود در پایان هر آنالیز ، ستون با حجمی از حلال معادل ۱۰ – ۲۰ برابر حجم ستون ( حداکثر تا ۲۵ میلی متر حلال یا ۲۵ دقیقه با سرعت جریان ۱ میلی متر در دقیقه ) شسته شود.
۵- در بسیاری از موارد آنالیز مواد با HPLC به حرارت حساس میباشد. از این رو توصیه میشود تا حد امکان دمای ستون کنترل شود .
۶ – هر نمونه ای را به ستون تزریق نکنید. توصیه میشود فقط نمونه های تمیز را به دستگاه تزریق کنید . حلالهای مورد استفاده در تهیه فاز متحرک و حل کردن نمونه ها از نظر خلوص باید مناسب باشند. همواره از آب مقطر دوبار تقطیر استفاده کنید .
8 – صاف کردن نمونه ها و فاز متحرک قبل از تزریق به دستگاه از ضروریات نگهداری یک ستون است.
۹- اگر یک ستون HPLC درست به کار گرفته شود. بطور معمول می توان ۲۰۰۰- ۵۰۰۰ نمونه را با آن آنالیز کرد .
توصیه میشود پیش از آنکه علایم از کار افتادن ظاهر شوند. ستون را کنار بگذارید.


